会议回顾
2025年1月17日,应Guangzhou RNA Club邀请,中国科学院生物物理研究所王艳丽教授作了题为 “The RNA-guided arms race between bacteria and phages” 的线上学术报告。王艳丽教授是国家“杰出青年科学基金”获得者、长江学者,长期从事CRISPR-Cas系统及其调控机制的研究,主要聚焦以下四个方向:(1) 第一类CRISPR-Cas系统的作用机理;(2) 第二类CRISPR-Cas系统的作用机理;(3) Anti-CRISPR蛋白对CRISPR活性的抑制机制;(4)小分子介导的基因沉默的结构生物学研究。
会议内容
在本次报告中,王艳丽教授围绕CRISPR-Cas 免疫系统的作用原理及其与噬菌体的对抗展开,重点介绍了 CRISPR-Cas 的分类、作用机制,以及细菌与噬菌体之间的进化博弈,特别是噬菌体如何通过 Anti-CRISPR(ACR)蛋白规避 CRISPR-Cas 系统的攻击,为 CRISPR-Cas 相关调控研究提供了新的视角。
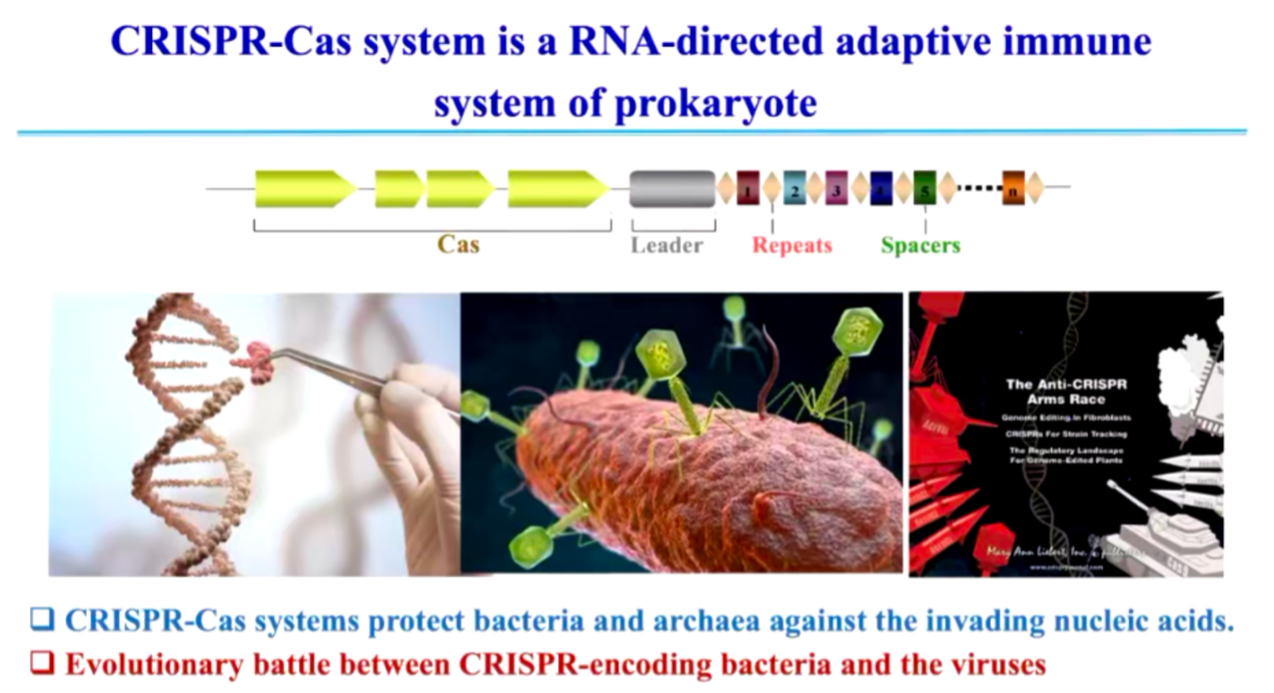
图1. CRISPR-Cas 系统及其进化军备竞赛
一、CRISPR-Cas 免疫系统的基础
1. CRISPR-Cas 系统概述
CRISPR-Cas 系统是一种 RNA 介导的获得性免疫系统,广泛存在于细菌和古细菌中 (图1)。它能够识别并降解入侵的外源 DNA,以抵御噬菌体感染。除此之外,CRISPR-Cas 由于其高度的靶向性,被发展为强大的基因编辑工具,在生命科学、医学和农业等领域发挥重要作用。
2. CRISPR-Cas 的作用机制
CRISPR-Cas 系统通过“记忆 - 识别 - 降解”的方式对抗噬菌体入侵,其作用过程可分为三个阶段 (图2):
适应 (Adaptation): 细菌在噬菌体首次入侵时,会截取一小段噬菌体 DNA 片段,并将其作为间隔序列 (spacer)整合到宿主 CRISPR 基因座中,相当于存储入侵者的“身份信息”。
表达 (Expression): 这些存储的 DNA 片段会被转录生成前体 crRNA (pre-crRNA),再经过加工形成成熟的 crRNA,携带间隔序列信息。
干扰 (Interference): 成熟 crRNA 结合 Cas 蛋白,形成效应复合物,一旦识别到匹配的噬菌体 DNA,就会触发核酸内切酶活性,靶向降解入侵 DNA,从而阻止噬菌体复制。
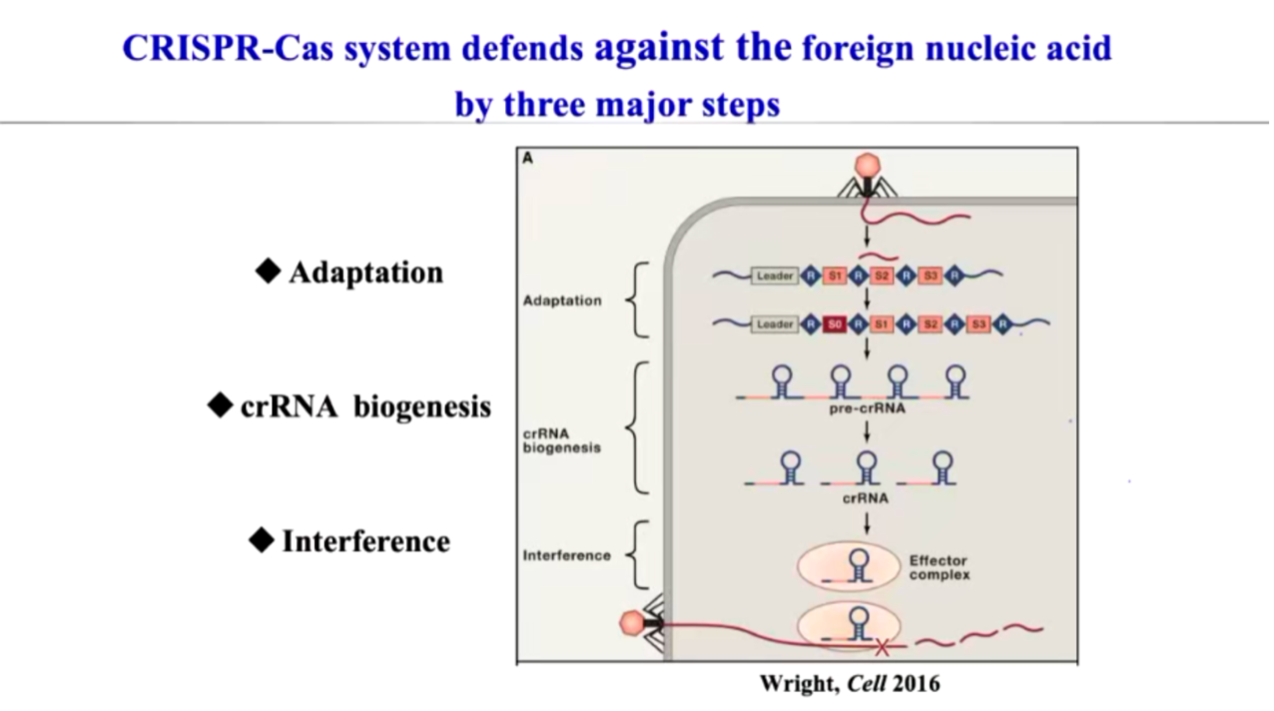
图2. CRISPR-Cas 系统的三大防御步骤
3. CRISPR-Cas 的分类
根据 Cas 蛋白的组成,CRISPR-Cas 系统被划分为两大类 (Class 1 和 Class 2) (图3):
第一大类 (Class 1)由多个 Cas 蛋白共同组成,与 crRNA 结合形成大型蛋白-RNA 复合物,包括 Type I、Type III 和 Type IV。其中 Type I 是最早被发现的 CRISPR-Cas 系统,也是自然界中分布最广泛的类型,约 90% 的 CRISPR-Cas 系统属于该类,主要依赖 Cas3 进行 DNA 降解。
第二大类 (Class 2)由单个大型 Cas 蛋白负责 crRNA 结合和 DNA 识别切割,结构更简洁,包括 Type II、Type V 和 Type VI。其中 Type II 是 CRISPR 研究中的重要类别,其代表性蛋白 Cas9 已被广泛应用于基因编辑技术,推动了生命科学和医学领域的发展。

图3. 糖RNA的实验策略CRISPR-Cas 系统的分类及其类型特征
二、不同 CRISPR-Cas 系统的作用机制
1. Type I CRISPR-Cas (Class 1)
Type I CRISPR-Cas (Class 1)主要依赖 Cas3 进行 DNA 降解。该系统由多个 Cas 蛋白与 crRNA 形成大型复合物,首先识别带有 PAM (Protospacer Adjacent Motif)序列的靶 DNA (图4)。识别后,会招募 Cas3,Cas3 能够沿 DNA 移动并持续降解大片段 DNA (图5)。这种降解模式不同于 Type II (Cas9)系统的精准切割。
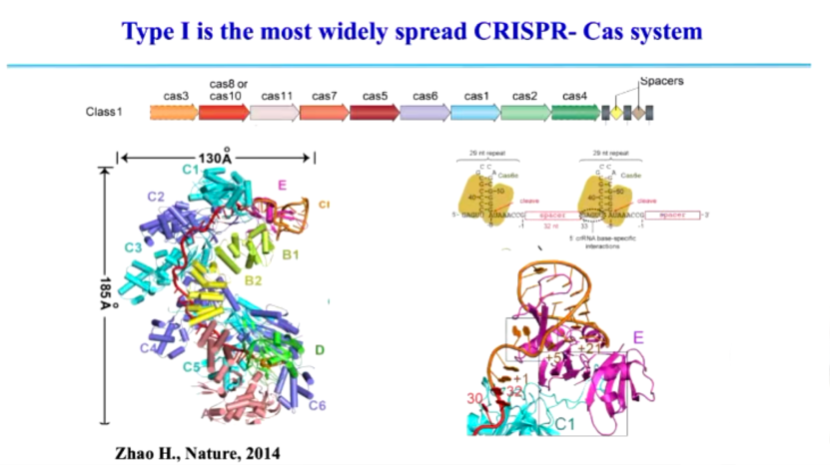
图4. Type I CRISPR-Cas 系统的工作机制
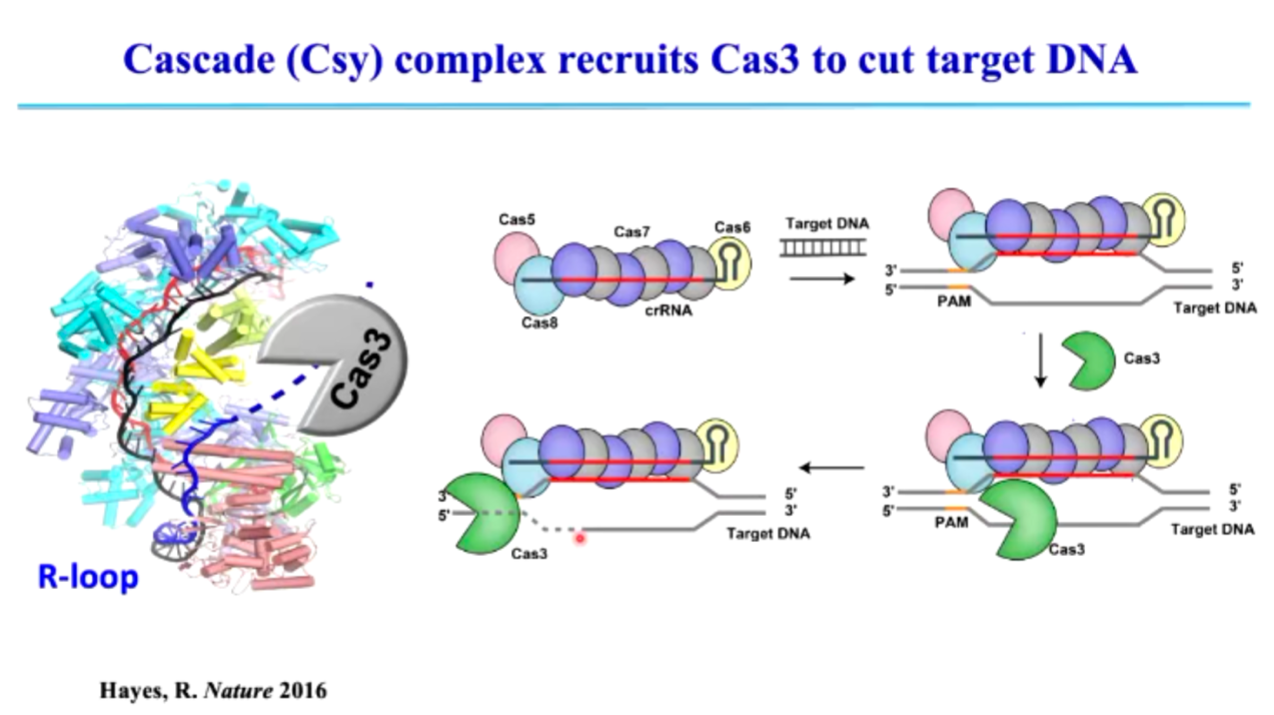
图5. Cascade 复合体招募 Cas3 切割目标 DNA
2. Type II CRISPR-Cas (Class 2)
相比之下,Type II CRISPR-Cas (Class 2)主要依赖 Cas9 进行 DNA 切割。Cas9 介导的免疫过程中 (图6, 图7),首先结合 sgRNA,形成蛋白-RNA 复合物。随后识别目标 DNA 并形成 R-loop 结构。最终,HNH 结构域和 RuvC 结构域分别切割互补链和非互补链,完成 DNA 断裂。
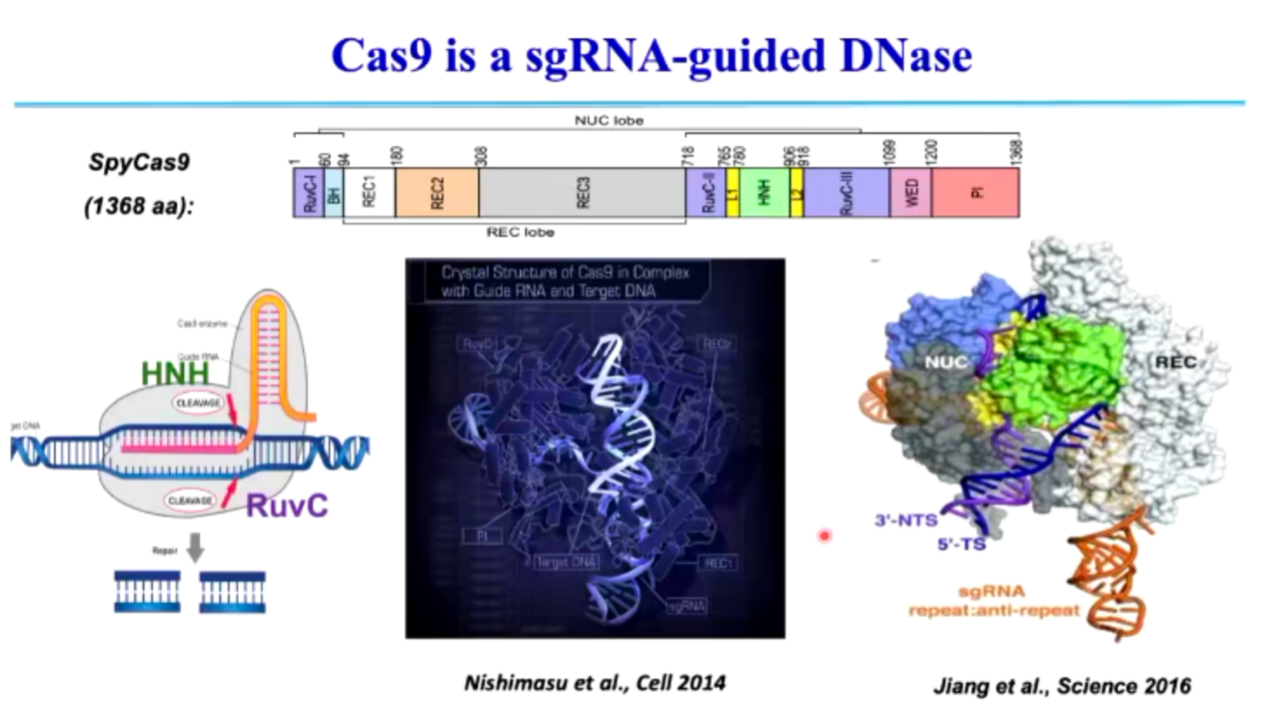
图6. Cas9 结构域及 DNA 切割机制
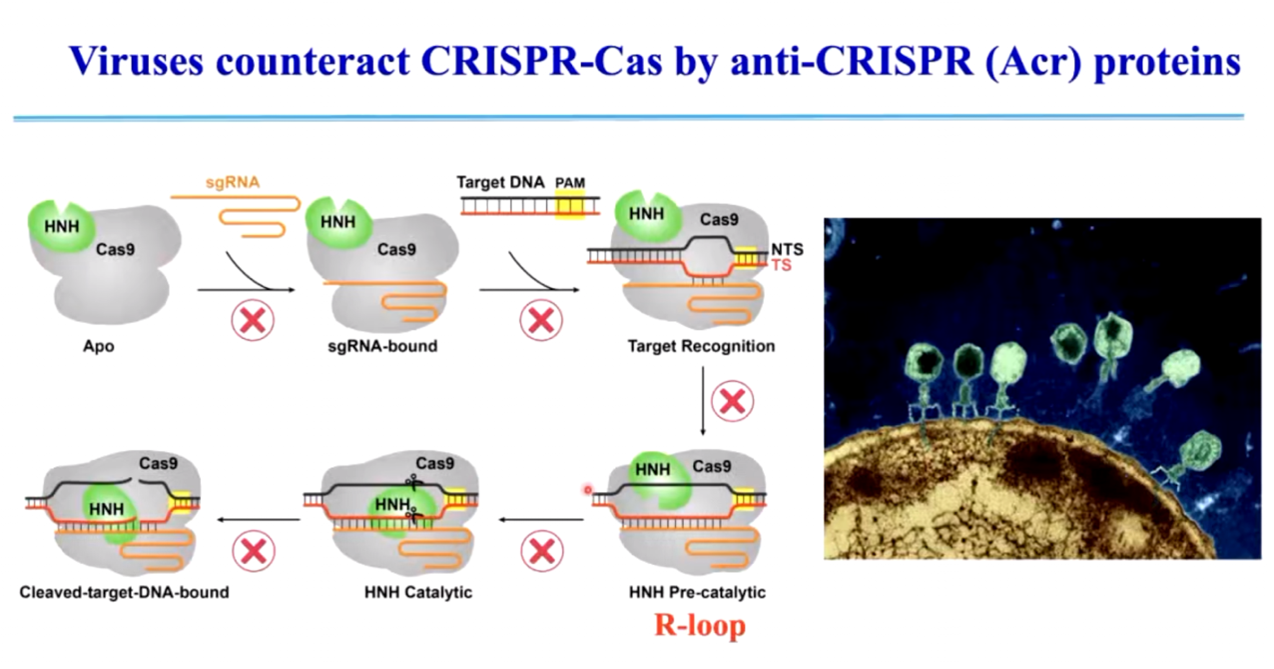
图7. Cas9 识别并切割 DNA 的动态过程
三、细菌与噬菌体的“军备竞赛”
尽管 CRISPR-Cas 赋予细菌强大的免疫能力,但噬菌体作为进化速度极快的病毒,也在不断演化出逃避免疫识别或直接抑制 CRISPR 活性的策略,使得细菌与噬菌体之间形成了一场持续的“军备竞赛”。在这一竞争过程中,噬菌体不断优化自身基因组,以逃脱 CRISPR-Cas 免疫系统的监测,而细菌则不断优化 CRISPR-Cas 机制,以维持其防御能力。噬菌体的主要对抗策略包括两种:
突变免疫逃逸:噬菌体通过基因组突变,改变其 DNA 序列,使其不再被 CRISPR-Cas 识别,从而成功逃避降解。这种策略依赖于噬菌体高突变率,能够在短时间内适应细菌的免疫防御。
Anti-CRISPR (ACR) 蛋白抑制:噬菌体进化出 Anti-CRISPR(ACR)蛋白,能够直接抑制 CRISPR-Cas 复合物的功能,阻止其识别、靶向或降解噬菌体 DNA。ACR 蛋白在噬菌体与宿主的长时间博弈中逐渐演化而来,成为噬菌体抵抗 CRISPR-Cas 免疫的关键武器。
四、噬菌体的 Anti-CRISPR (ACR)机制
ACR 蛋白是噬菌体对抗 CRISPR-Cas 免疫系统的重要策略,它们通过不同方式阻碍 CRISPR-Cas 的活性,针对不同类型的 CRISPR-Cas 体系,ACR 蛋白的抑制策略也有所不同。目前,研究表明,ACR 主要通过以下方式抑制 Type I(Class 1)和 Type II(Class 2)CRISPR-Cas 系统。
1. ACR 对 Type I CRISPR-Cas 的抑制机制
Type I CRISPR-Cas 系统主要依赖 Cascade 复合物(由多个 Cas 蛋白与 crRNA 组成)识别靶 DNA,并通过 Cas3 进行 DNA 降解。ACR 蛋白的主要抑制策略是干扰 Cascade 复合物的组装或阻断 Cas3 的招募,从而削弱 CRISPR-Cas 的免疫能力。
(1)AcrIF25: 破坏 Cascade 复合物的稳定性,使 CRISPR-Cas 失去识别与降解功能 (图8)。
在 Type I CRISPR-Cas 系统中,Cascade 复合物由多个 Cas 蛋白 (包括 Cas7)与 crRNA 共同组成,能够精确靶向噬菌体 DNA,并招募 Cas3 进行降解。而 AcrIF25 通过特异性结合 Cas7,破坏 Cascade 复合物的结构,使其无法稳定结合 crRNA 和靶 DNA。这种结构的不稳定性导致 crRNA 无法精准匹配目标序列,进而影响 Cas3 的招募,使 CRISPR-Cas 复合物 丧失降解噬菌体 DNA 的能力,最终让噬菌体成功规避宿主免疫系统。
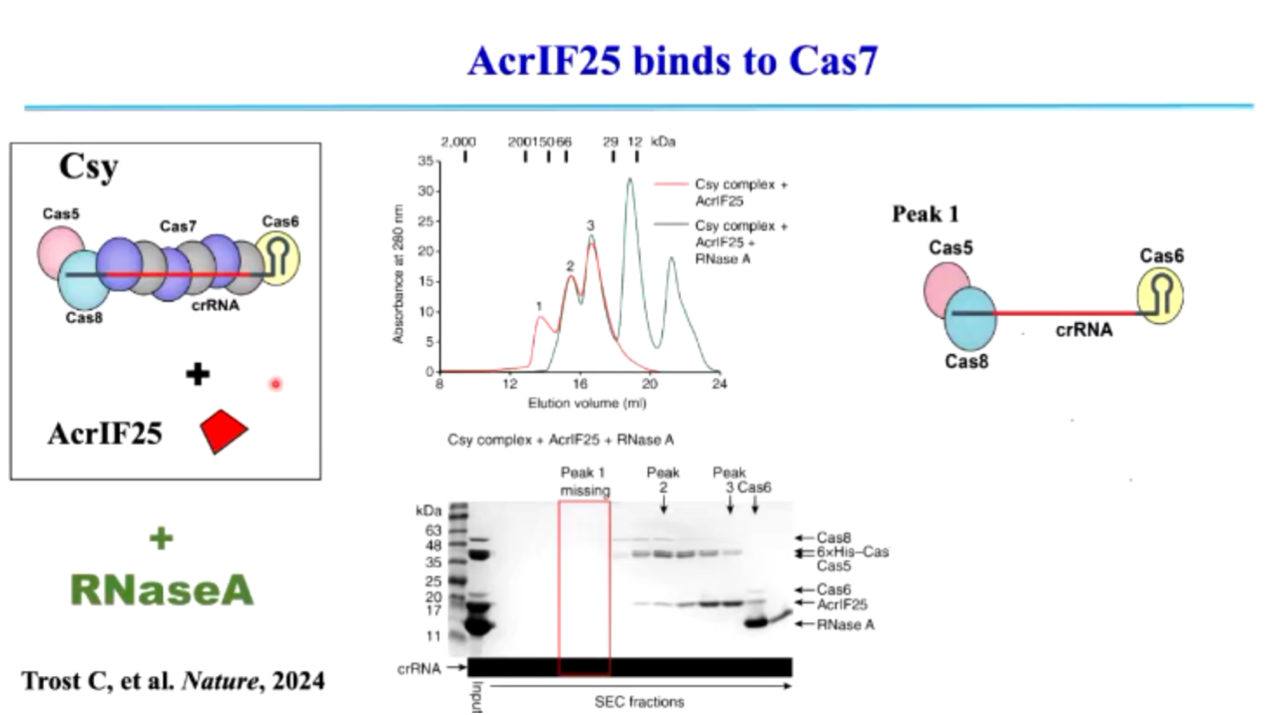
图8. AcrIF25 与 Cas7 结合,影响 CRISPR-Cas 系统功能
(2) AcrIF3: 通过阻断 Cas3 的招募,抑制 CRISPR-Cas 介导的 DNA 降解 (图9)。
在 Type I CRISPR-Cas 免疫过程中,Cascade 复合物在识别到靶 DNA 后,需要招募 Cas3 作为核酸酶执行 DNA 降解。而 AcrIF3 通过直接结合 Cas3,阻止其与 Cascade 复合物相互作用,使 Cas3 无法被正确招募。由于 Cas3 无法执行降解任务,即便 Cascade 复合物仍然能够识别噬菌体 DNA,宿主也无法清除入侵的外源基因组,从而使噬菌体 DNA 得以复制,成功逃避免疫攻击。
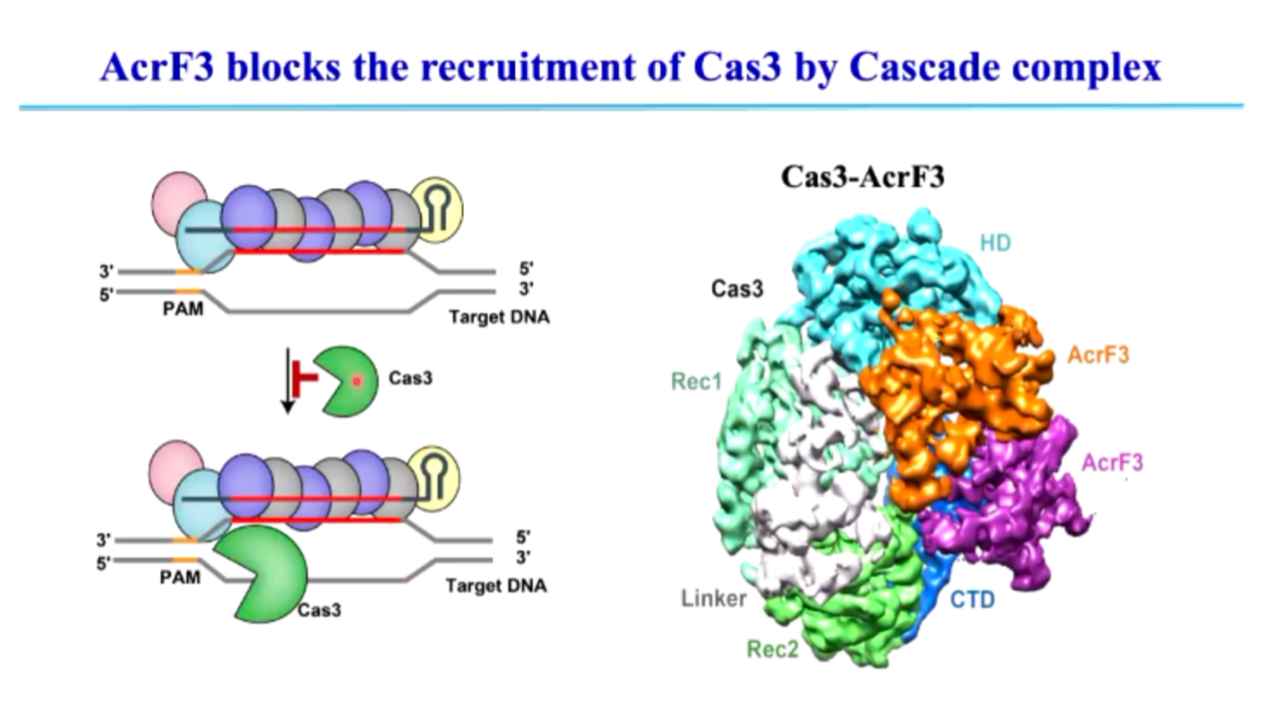
图9. AcrF3 阻止 Cas3 被 Cascade 复合体招募
2. ACR 对 Type II CRISPR-Cas 的抑制机制
Type II CRISPR-Cas 系统依赖 Cas9 进行 DNA 识别和切割,ACR 蛋白的抑制策略主要针对 sgRNA 结合、DNA 结合位点竞争、R-loop 结构形成及 Cas9 的构象变化等关键环节。
(1)AcrIIC2: 结合 Cas9 的 Bridge Helix(BH)结构域,阻止 sgRNA 结合,使 CRISPR-Cas 丧失 DNA 识别能力 (图10)。
Cas9 需要依赖 sgRNA 结合并引导 DNA 识别,其中 BH 结构域(Bridge Helix)是 Cas9 结合 sgRNA 的关键 α 螺旋结构。AcrIIC2 通过结合 Cas9 的 BH 结构域,形成二聚体,占据 sgRNA 结合位点,使 Cas9 无法加载 sgRNA,进而阻止 DNA 识别。这种抑制作用直接作用于 CRISPR-Cas 免疫过程的最早阶段,使 Cas9 在免疫反应的初始阶段就处于完全非活性状态,最终使细菌失去对噬菌体 DNA 的防御能力 (图10)
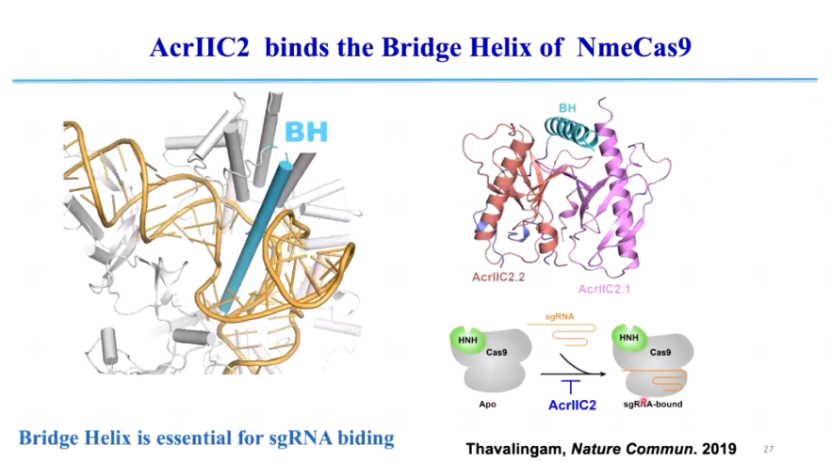
图10. AcrIIC2 结合 BH 阻碍 Cas9 激活
(2)AcrIIC5: 通过竞争 Cas9 的 DNA 结合位点,使 Cas9 误结合错误靶点,阻止其识别真实的目标 DNA (图11)。
在正常情况下,Cas9 通过识别 PAM(Protospacer Adjacent Motif)序列进行 DNA 结合,而 AcrIIC5 由于表面带有类似双链 DNA(dsDNA)的酸性区域,能够模拟 DNA 结构,与 Cas9 结合,使其误认为 AcrIIC5 是目标 DNA。被误导的 Cas9 无法识别真正的噬菌体 DNA,导致 CRISPR 免疫系统无法启动降解程序,从而使噬菌体成功逃避攻击。
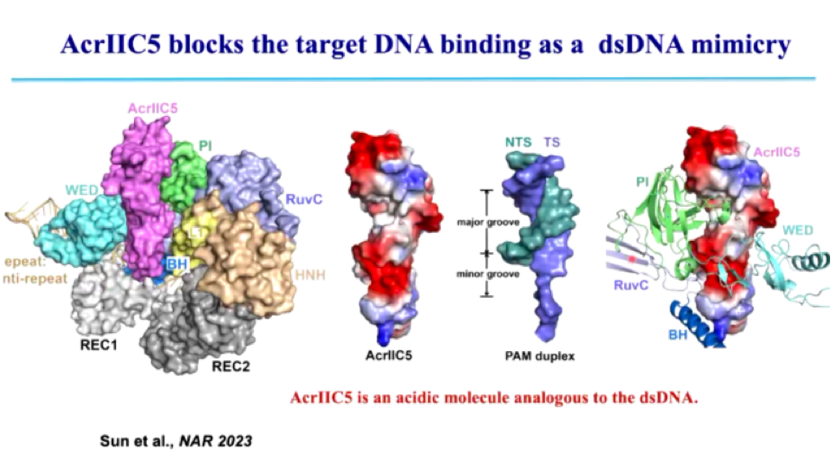
图11. AcrIIC5 通过模拟 DNA 阻止 Cas9 识别靶 DNA
(3) AcrIIC4: 通过阻碍 R-loop 结构的形成,使 Cas9 处于非活性状态,无法执行 DNA 切割 (图12, 图13)。
在正常的 CRISPR 免疫过程中,Cas9 识别 DNA 后,sgRNA 会与靶 DNA 形成 R-loop 结构,这一结构的稳定形成是 Cas9 介导 DNA 切割的关键步骤。而 AcrIIC4 通过嵌入 Cas9 REC1 和 REC2 结构域之间的缝隙,阻止 Cas9 结构域的运动,使 Cas9 无法完成构象变化。由于 Cas9 结构受到抑制,R-loop 结构无法正确形成,Cas9 也无法完成 DNA 断裂,最终噬菌体 DNA 得以存活并复制。
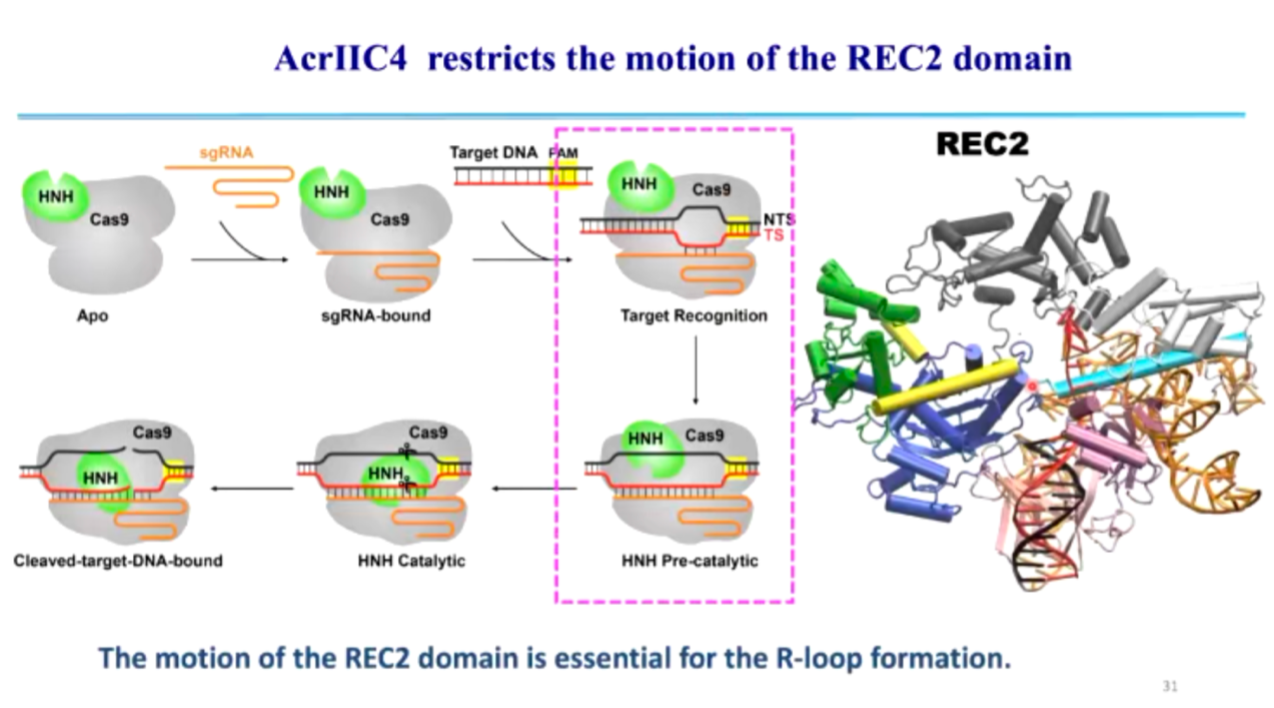
图12. AcrIIC4 限制 REC2 运动,阻止 R-loop 形成
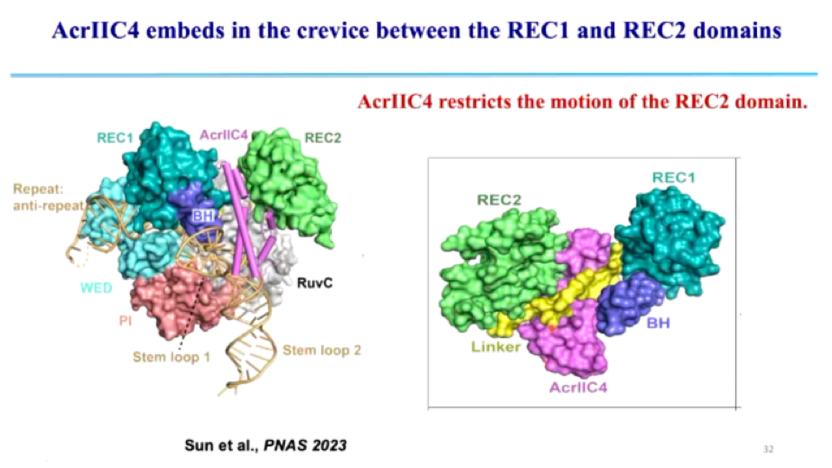
图13. AcrIIC4 嵌入 REC1 和 REC2 之间抑制 Cas9
(4) AcrIIC3: 结合 Cas9 的 HNH 结构域和 R2 结构域,锁定 Cas9 在非活性构象,使其无法切割 DNA (图14)。
Cas9 在执行 DNA 切割时,HNH 结构域需要进行大幅度旋转,从非活性状态转变为活性状态,才能执行精确的 DNA 切割。而 AcrIIC3 通过结合 Cas9 的 HNH 结构域和 R2 结构域,形成稳定的二聚体,使 Cas9 结构域无法发生必要的构象变化。这种分子锁定机制使 Cas9 即便已经结合 sgRNA 和 DNA 仍无法激活核酸酶活性,从而阻止 DNA 降解,使噬菌体 DNA 免受 CRISPR-Cas 免疫系统的攻击。
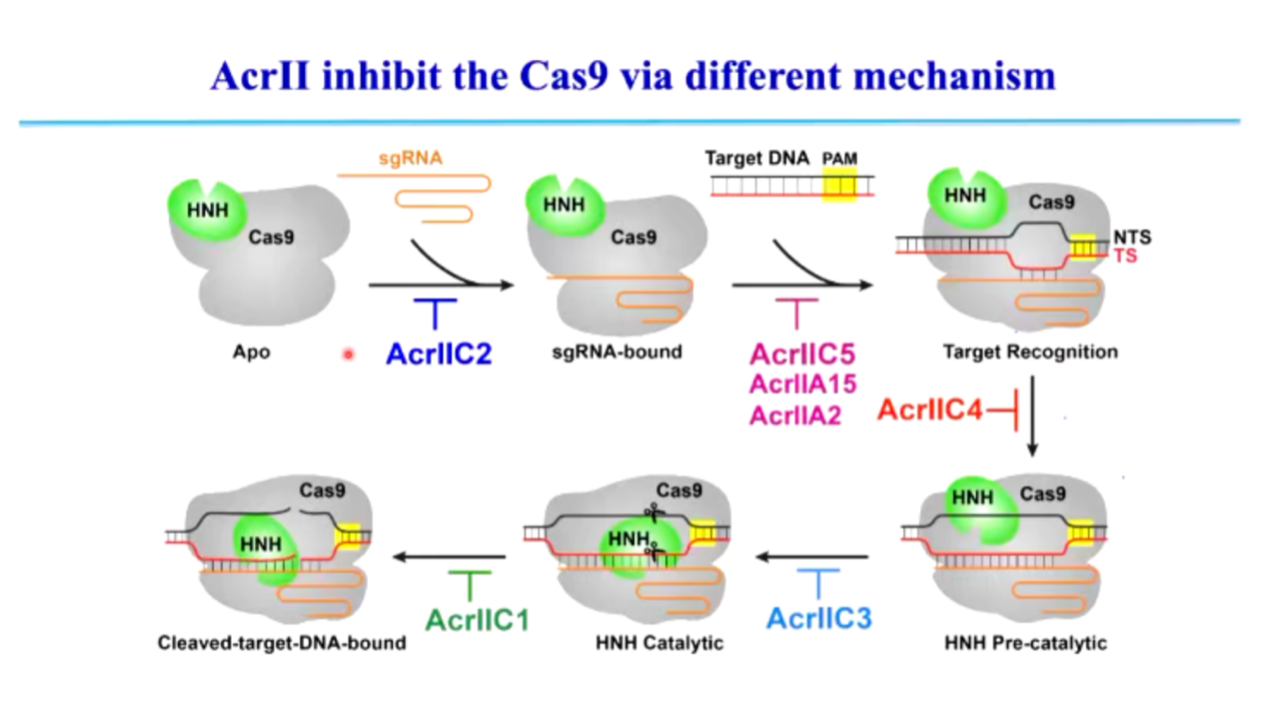
图14. 不同 ACR 蛋白抑制 Cas9 的多种机制
CRISPR-Cas 系统在细菌和古细菌中作为重要的免疫防御工具,其多样化的作用机制赋予了它强大的适应性。然而,噬菌体也在不断进化,通过突变逃逸和 Anti-CRISPR 机制对抗 CRISPR-Cas,形成了生物学上的“军备竞赛”。这些研究不仅加深了我们对 CRISPR-Cas 免疫系统的理解,也为基因编辑技术的改进和 CRISPR-Cas 相关调控策略的开发提供了新的研究方向。
精彩问答
问题1:噬菌体的抑制机制为何要组装好后又拆除?这种机制是否用于维持平衡?
答:噬菌体编码的蛋白,如 F25,能够抑制 CRISPR-Cas 系统,从而抵抗宿主的免疫机制。这种机制类似于病毒与宿主之间的对抗关系,如新冠病毒与人体免疫系统的互相适应。
问题2:抑制 CRISPR-Cas 的因子主要是来自噬菌体的基因组吗?
答:目前研究发现,大多数抑制因子都是噬菌体编码的蛋白,但也有一些 RNA 分子可以模拟 CRISPR-Cas 结构并进行抑制。
问题3:anti-CRISPR 机制在不同阶段的作用强度如何?在哪个阶段抑制效果最好?
答:最有效的抑制方式是干扰 CRISPR-Cas 复合物与 DNA 的结合。这一机制已被多个不同的 anti-CRISPR 蛋白所利用,尽管它们的具体作用机制各不相同。
问题4:在人类和哺乳动物细胞中进行 CRISPR 基因编辑时,是否存在类似的 anti-CRISPR 机制?
答:哺乳动物细胞自身并不具有天然的 anti-CRISPR 机制,但可以通过人为设计来调控 CRISPR 编辑,例如设计调控 CRISPR 活性的蛋白或 RNA 分子,从而实现对基因编辑的精确控制。
问题5:AI 是否可以用于预测新的 anti-CRISPR 蛋白?目前对 anti-CRISPR 蛋白的研究是否还不完整?
答:目前已知的 anti-CRISPR 蛋白种类仍然较少。自 2016 年首次发现以来,研究进展迅速,但仍有许多未知的机制。AI 可以用于预测更多可能的 anti-CRISPR 蛋白,并帮助发现新的作用模式。
问题6:细菌自身是否存在针对 anti-CRISPR 的调控机制?
答:细菌确实存在调控 anti-CRISPR 的机制。例如,一些蛋白可以结合 anti-CRISPR 蛋白的启动子,抑制其表达,从而调控 CRISPR-Cas 系统的活性。这可能有助于维持宿主与噬菌体的平衡。
问题7:CRISPR-Cas 系统在解析 MEME 与 Cas9 复合物的结构时,是否能观察到完整的 HNH 结构?
答:由于研究采用的是晶体结构解析技术,因此能够以高分辨率解析 HNH 结构域的每个原子,包括结合的金属离子,所有氨基酸侧链的密度都吻合良好。
问题8:这种 HNH 结构是如何捕捉到的?是在样品制备过程中获得的稳定状态,还是通过构象分类发现的瞬时状态?
答:研究人员在制备过程中采用了突变小蛋白,并结合特定的实验条件,从而成功捕捉到了 HNH 结构的活性状态,虽然其中有一定的运气成分,但实验设计在稳定性控制方面发挥了重要作用。
问题9:anti-CRISPR 蛋白的不同类型是否存在进化关系?它们的结构域是否具有保守性?
答:anti-CRISPR 蛋白具有极高的多样性,不同种类之间的结构域并没有明显的保守性。这种多样性类似于病毒的进化模式,即生物越低等,其基因和蛋白的多样性就越高。
Yanli Wang教授此次会议报告已收录于Guangzhou RNA club bilibili视频网站(【王艳丽-RNA引导的细菌和噬菌体之间的军备竞赛】 https://www.bilibili.com/video/BV1EicdeSEsQ/?spm_id_from=333.1387.homepage.video_card.click&vd_source=14c9f25d8be80315627a81e27b88ba71)
欢迎关注Guangzhou RNA club公众号、网站(rnaclub.rnacentre.org)、twitter(@RNA_club)。













