会议回顾
2024年8月29日,美国斯坦福大学的李进(Jin Billy Li)教授受邀在Guangzhou RNA club进行了题为“RNA Editing: Innate Immunity and Antoinflammatory Disease”的线上学术报告。Billy教授于2010年起加入斯坦福大学建立实验室,实验室研究重点是ADAR酶介导的RNA编辑,实验室发现RNA编辑在避免双链RNA介导的自身免疫中的重要生物学作用,这一发现为癌症和自身免疫性疾病治疗的创新方法铺平了道路。实验室的另一个主要方向是利用内源性ADAR酶开发定点RNA碱基编辑技术,该方法克服了CRISPR/Cas DNA编辑相关的挑战,为解决罕见和常见疾病带来了新的希望。Billy教授近年来在Nature,Science,Nature Biotechnology、Nature Methods等期刊发表了多篇高水平论文。
会议内容
本次会议中,Billy教授主要围绕ADAR介导的RNA编辑在Double-stranded RNA(dsRNA)引起的先天性免疫和自身炎症性疾病中的作用展开阐述。
在生物体进化过程中,人类应对病原体的一个重要机制就是通过宿主体内的感受器(sensor)去识别病毒核酸(DNA or RNA)。这些感受器大多位于细胞质中,当有病毒入侵的时候,它首先进入的就是细胞的细胞质。这些感受器可分为dsDNA sensor和dsRNA sensor。
(1)dsDNA sensor:其中一个非常有名的dsDNA sensor是cGAS(环磷酸鸟苷-腺苷合成酶)。通过图1可知,当cGAS识别病原dsDNA后会激活cGAS-STING通路,进而激活下游的TBK1和IRF3,IRF3激活后会从胞质内入核促进I型干扰素的形成,从而实现一系列的抗病毒作用。
(2)dsRNA sensor:Billy教授主要介绍了2个dsRNA sensor:RIG-I和MDA5。RIG-I倾向于识别5’末端具有三磷酸基团(5’-PPP)或二磷酸基团(5’-pp)的短dsRNA;而MDA5倾向于识别较长的dsRNA和perfect-matched dsRNA,不在意其5’末端的序列。RIG-I和MDA5识别dsRNA以后会激活下游的MAVs,进而激活TBK1和IRF3,IRF3入核促进I型干扰素的产生,从而产生后续的抗病毒效应,见图1。
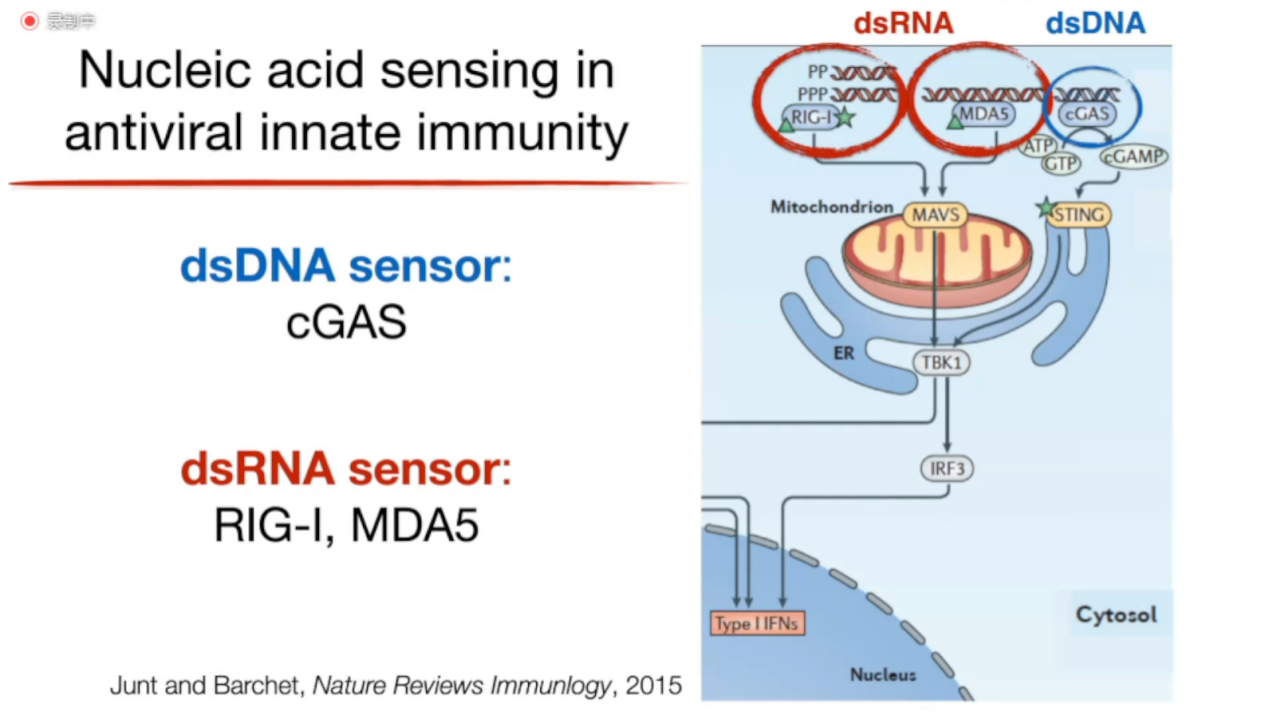
图1. dsRNA和dsDNA的sensor及信号通路
对于DNA而言,自身的DNA是在细胞核内,通常情况下自身DNA出现在细胞质中的概率较低;但是很多RNA转录以后会出核进入细胞质,大多数RNA会形成很长的dsRNA,并且这些dsRNA是来源于自身,而不是病毒的RNA,那么MDA5是如何避免去识别自身形成的dsRNA(内源dsRNA)呢?
Billy教授介绍了腺苷脱氨酶(ADAR),ADAR能够结合到内源dsRNA上,并对腺苷酸进行脱氨基反应,从而产生A to I RNA editing,I会被生物体识别为G,所以A to I产生的效应可以看作是A to G,正常情况下,ADAR1会编辑宿主自身的双链RNA,从而避免被MDA5识别。(图2)
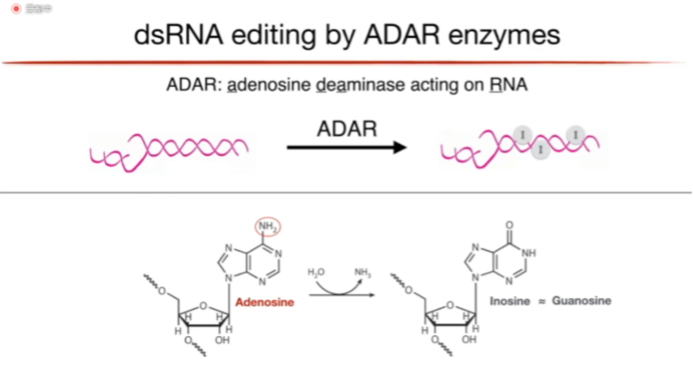
图2. ADAR的作用机制
在哺乳动物中,ADAR可以分为ADAR1和ADAR2,ADAR1又可以分为ADAR1p150和ADAR1p110(图3)。研究表明,同时敲除ADAR1的两种亚型后,小鼠在出生前就死亡了;后续有研究敲除了p150,但保留了p110,结果和同时敲除p150和p110几乎一样,说明ADAR1p150是非常重要的;敲除ADAR2,小鼠在出生后3周内也死亡了。ADAR1p150主要分布在细胞质中,ADAR1p110和ADAR2分布于细胞核内。(图4)
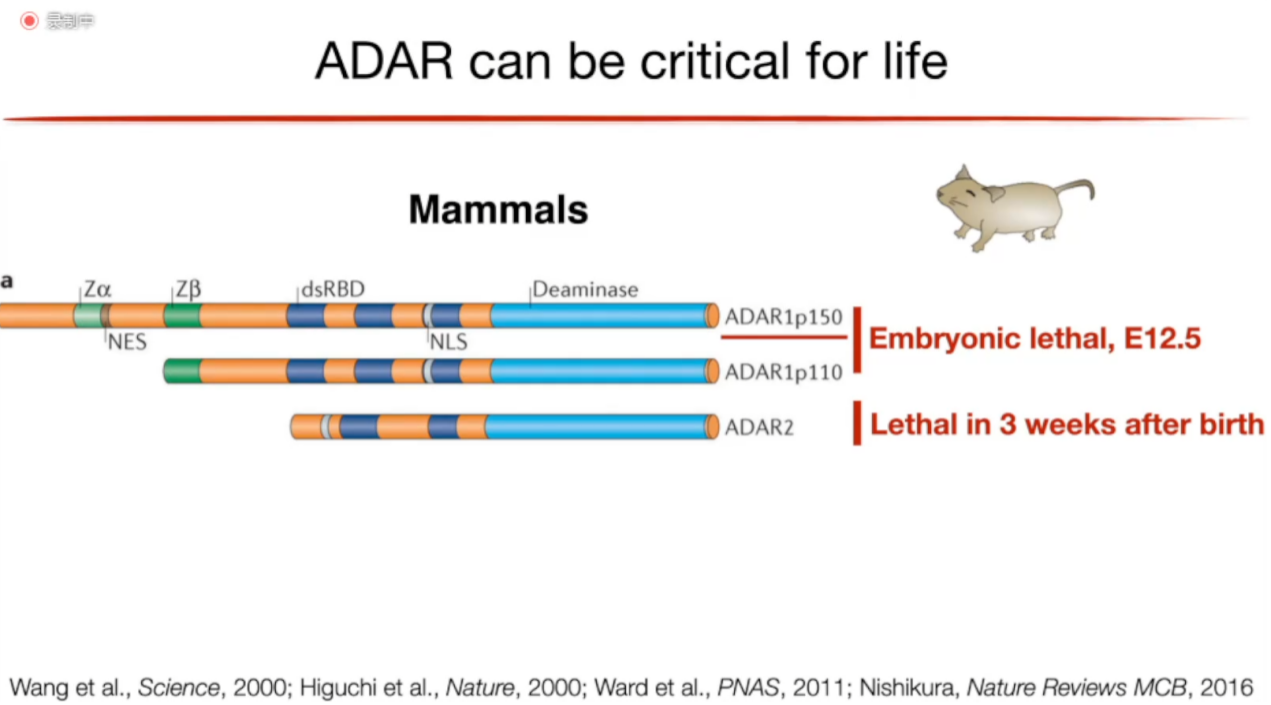
图3. 哺乳动物中ADAR的类型
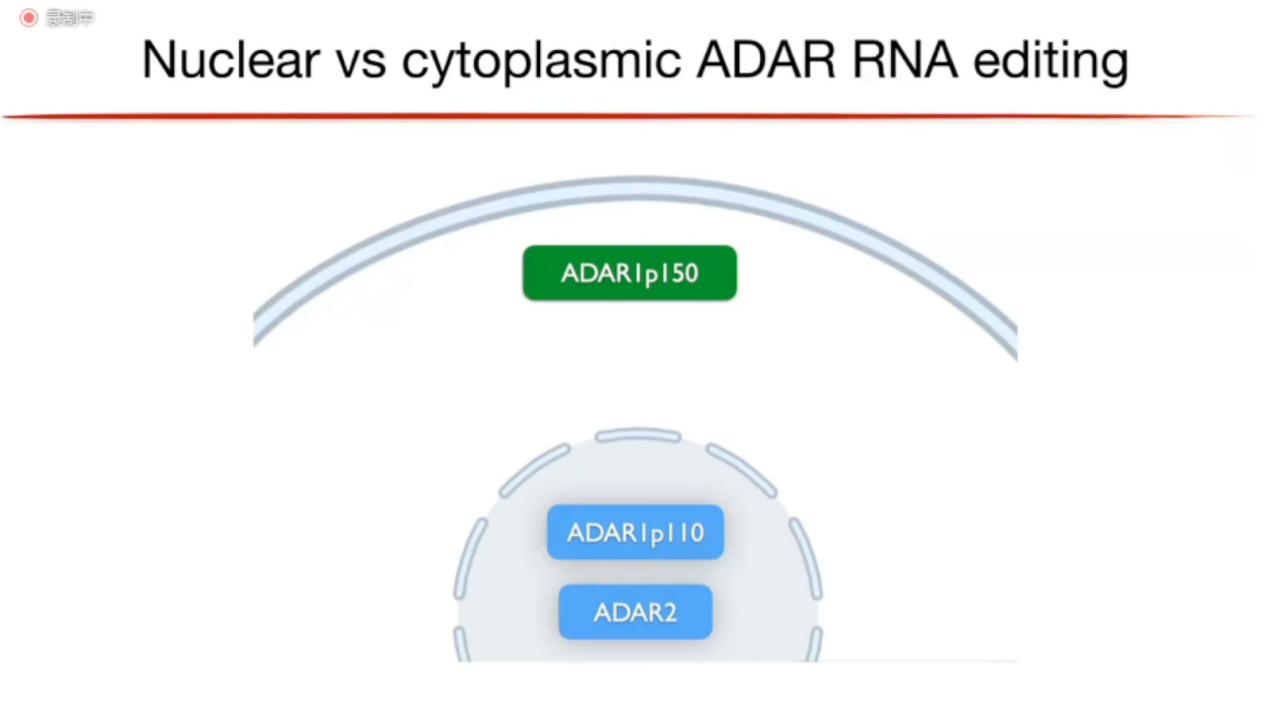
图4. 哺乳动物中ADAR的分布
Billy教授介绍目前在人类中找到的RNA editing事件至少有3百万个,但只有200多个编辑位点位于蛋白编码区域;绝大多数的编辑位点位于Alu区域,Alu相对于其它重复序列来说,拷贝数多,相似性更好,更容易形成很长很好的双链RNA。(图5)

图5. 编辑位点的分布情况
Billy教授介绍到早年有研究证明敲除ADAR1后,小鼠会在胚胎发育的12.5天死亡,如果敲除ADAR1的同时敲除MAD5,小鼠可以出生但只能存活2天,说明MDA5的激活可能与ADAR1有关。Billy教授团队与Carl Walkley合作,仅在ADAR1上发生E861点突变使ADAR1丧失编辑活性,但保留ADAR1蛋白,此时,小鼠也在胚胎发育的12.5天死亡,这能充分的说明(1)ADAR1的编辑功能非常重要;Billy教授团队在ADAR1发生点突变的基础上敲除MDA5,此时小鼠可以存活超过2年,这足以说明(2)ADAR1除了RNA编辑这个作用以外,还有其他原因影响了小鼠的寿命。(图6)
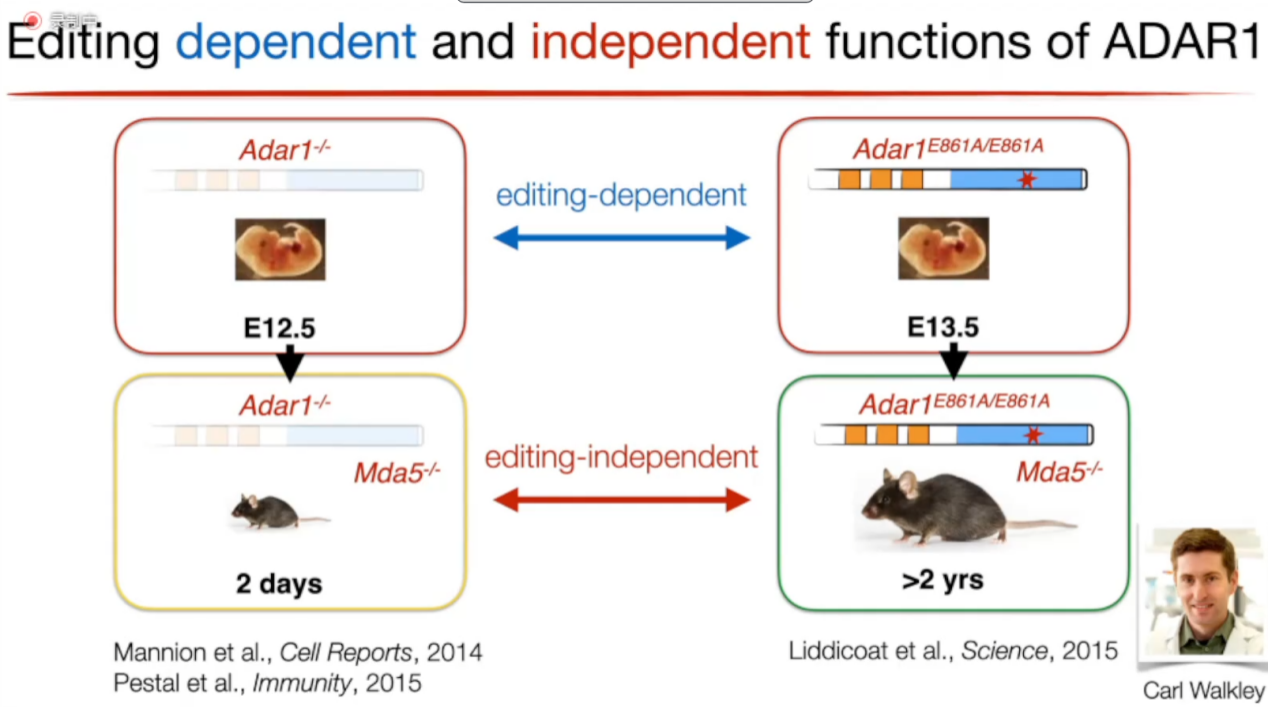
图6. ADAR1和MDA5改变对小鼠寿命的影响
Billy教授团队的博士后经过研究发现,在ADAR1和MDA5都被敲除之后,小鼠还是在出生后2天就死亡的原因是因为PKR被激活导致的。此时,Billy教授团队将ADAR1、MDA5、PKR都敲除,会发现有20%的小鼠都能存活2年以上了,但有80%在断奶前就死亡了。考虑到ADAR1有2种亚型,p150和p110,而RNA编辑是由存在于细胞质中的p150引起的,存在于细胞核中的p110不会对胞质中的RNA进行编辑,因此只敲除ADAR1p150而保留p110,此时所有的老鼠都可以存活正常的寿命。(图7)
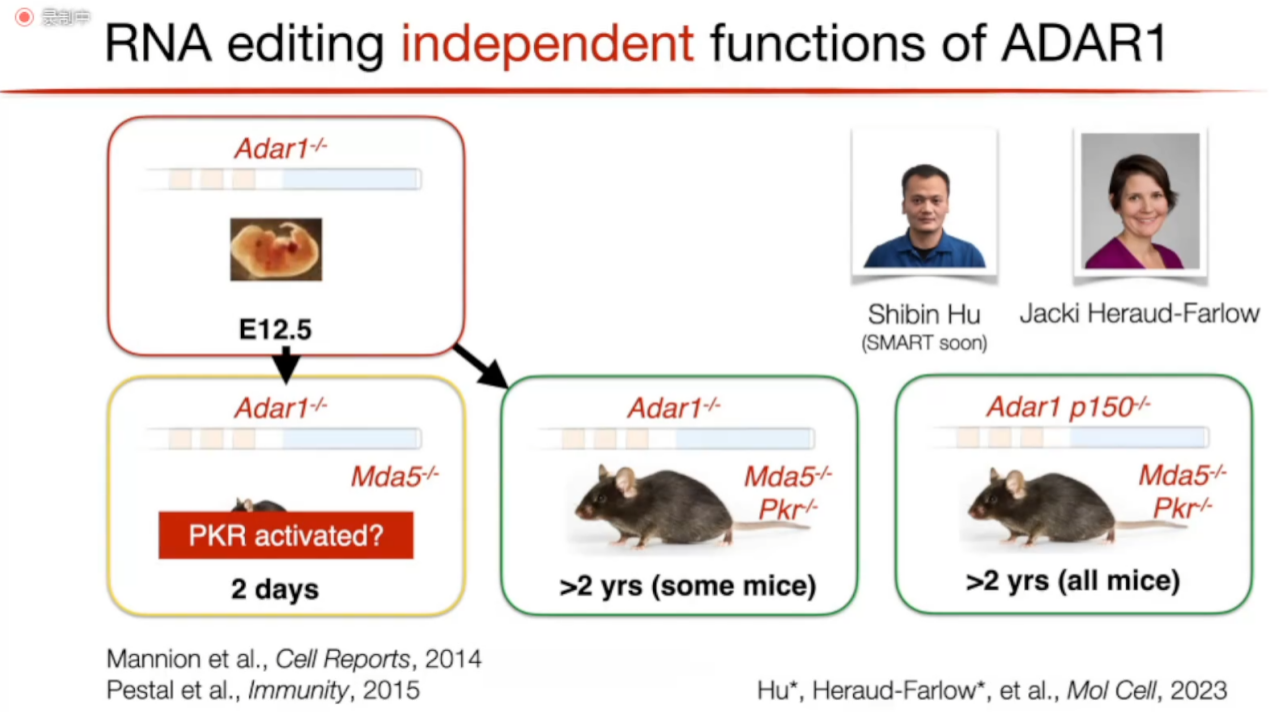
图7. PKR对小鼠寿命的影响
经过以上研究,可以证明ADAR1p150有2个主要的功能:(图8)
(1)RNA editing:ADAR1p150对dsRNA进行A to I编辑,导致MDA5不能将其识别,阻止了MDA5的激活。
(2)RNA binding:ADAR1p150与dsRNA进行结合,从而阻止了PKR与dsRNA结合,进而导致PKR不能被激活。
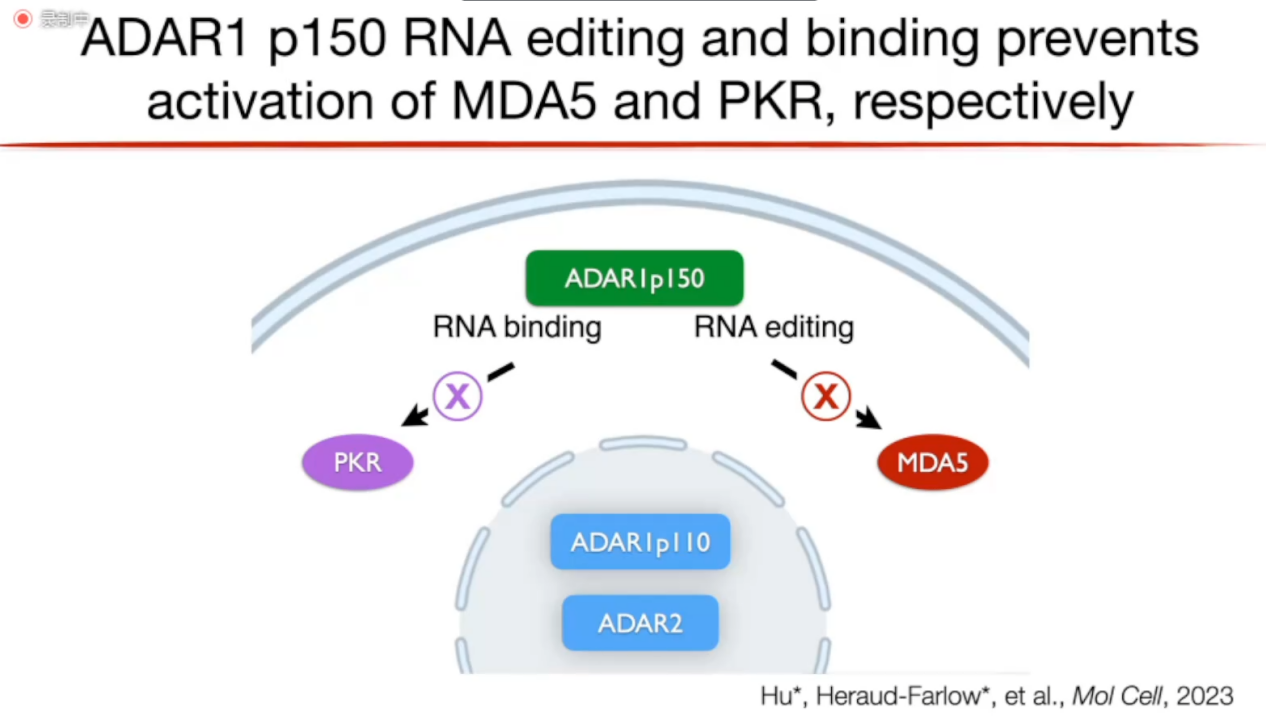
图8. ADAR1p150的主要功能
Billy教授强调了ADAR1最主要的功能就是对dsRNA进行编辑,防止MDA5被激活,如果dsRNA未被编辑,即使是内源性的dsRNA,也会激活MDA5。同时ADAR1功能丧失突变(LOF mutation)或者MDA5功能获得突变(GOF mutation)会导致一些罕见的自身免疫性疾病,比如Aicardi-Goutières综合症(AGS)。
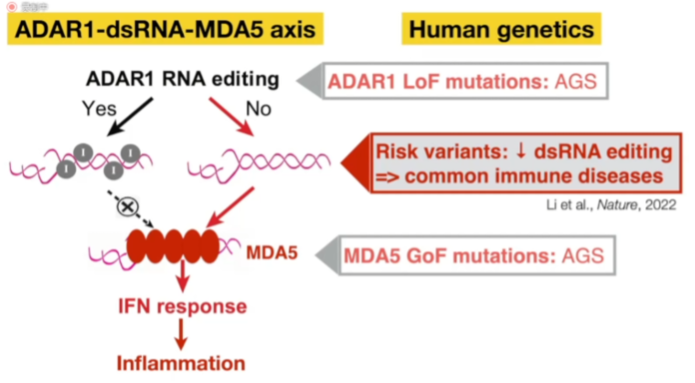
图9. ADAR1-dsRNA-MDA5通路
Billy教授介绍了他们团队在2022年完成的一项工作,他们基于完善的ADAR1-dsRNA-MDA5免疫通路,通过人类遗传学研究方法,发现了由遗传变异导致的双链RNA编辑水平下降是引发自身免疫病/炎症性疾病的一个重要机制。这些常见遗传变异在自身免疫病/炎症性疾病病人体内会同时降低免疫原性双链RNA的编辑水平,从而激发了由MDA5介导的干扰素免疫应答,最终引起慢性炎症反应。接下来,Billy教授详细的阐述了他们是如何发现这个结论的。
首先,他们进行了GWAS分析和RNA编辑性状座位分析(edQTL,RNA editing quantitative trait loci),共找到了超过3万个对RNA编辑水平有影响的edQTL(图10,图11)
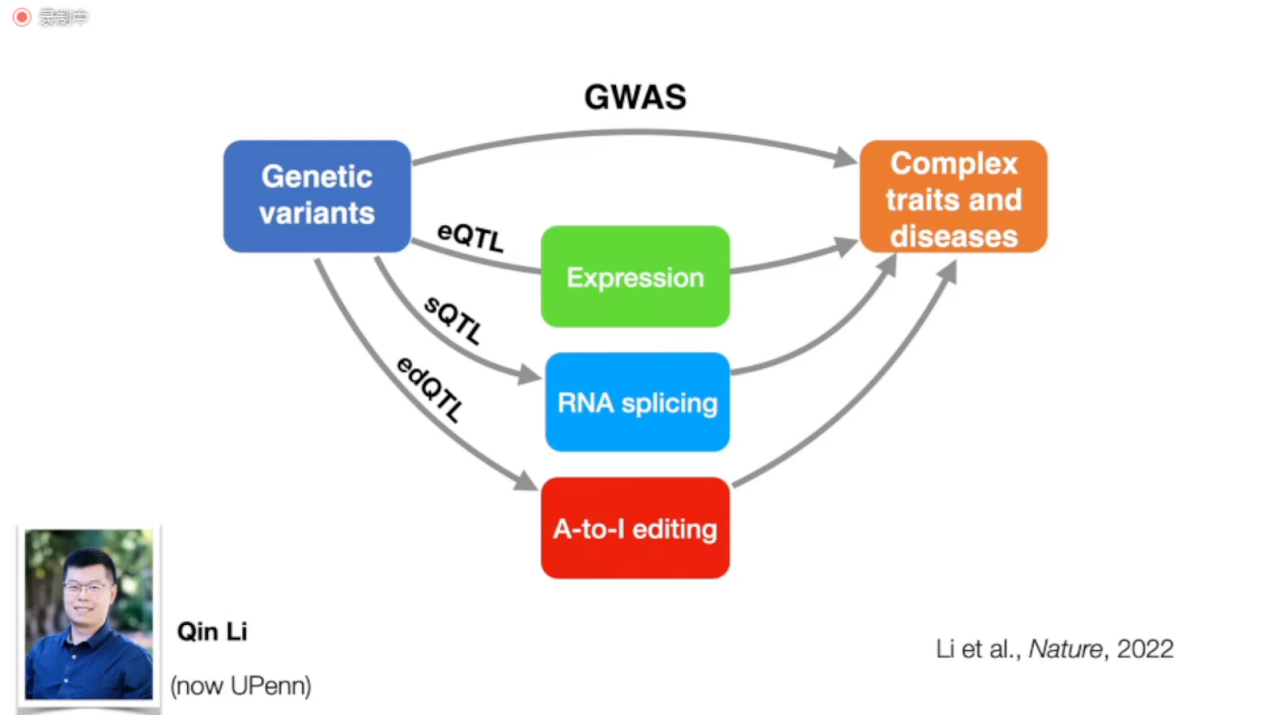
图10. 简要介绍eQTL,sQTL和edQTL
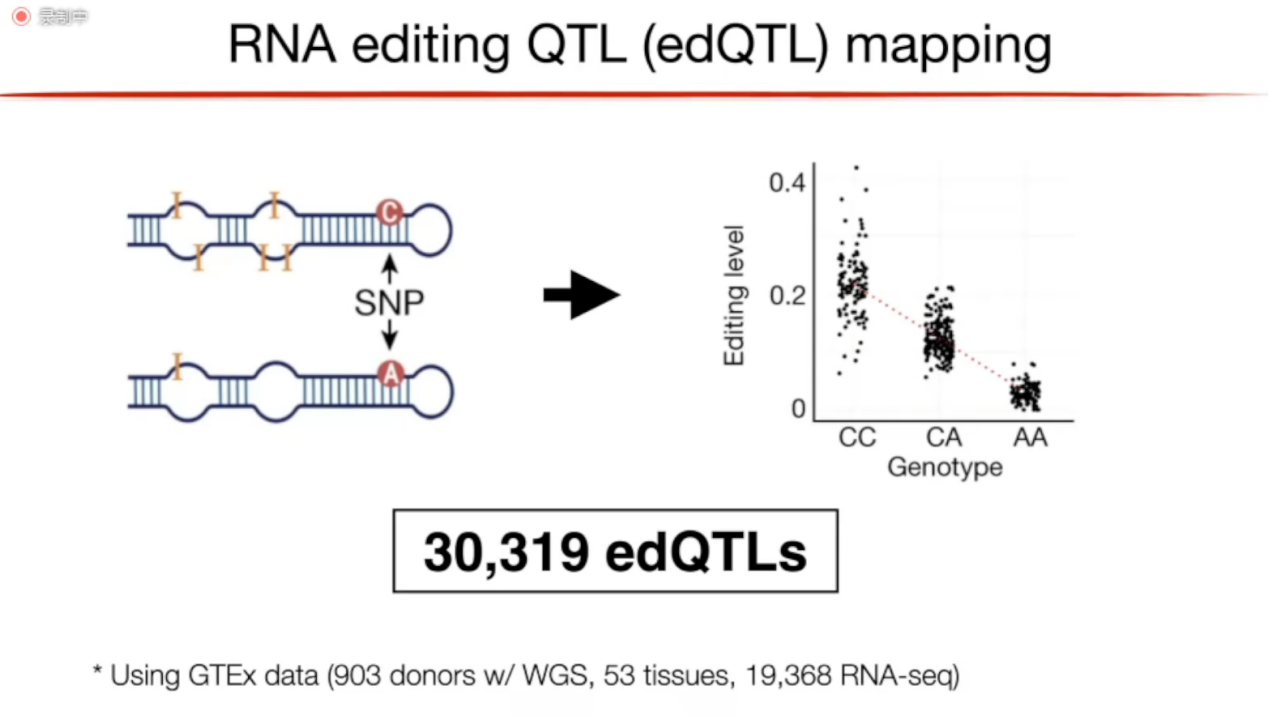
图11. edQTL举例
接下来,他们通过与大量人类疾病全基因组关联分析(GWAS),发现edQTL高度富集于自身免疫性疾病,比如系统性红斑狼疮、多发性硬化症、类风湿性关节炎等;包括和免疫功能相关的疾病,如冠心病等。(图12)
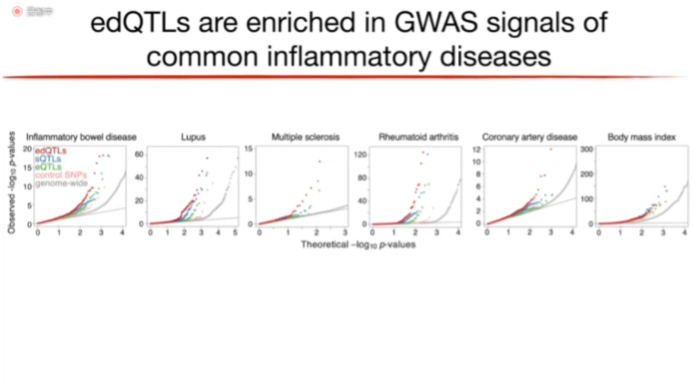
图12. GWAS分析发现edQTLs在炎症性疾病中富集
人体内能够被ADAR1编辑的dsRNA非常多,那么哪些dsRNA才是激活MDA5的关键底物呢?Billy教授团队对edQTL和GWAS数据进行了共定位(colocalization)分析来寻找这些免疫原性双链RNA(immunogenic dsRNA)。他们发现与疾病相关的免疫原性dsRNA绝大多数都位于Exon/UTR中;但在所有与edQTL相关的dsRNA中,接近2/3的dsRNA都位于Intron中。
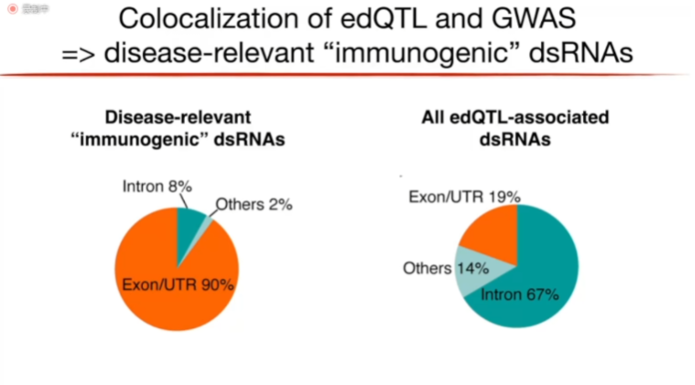
图13. 免疫原性dsRNA的分布情况
遗传变异是如何通过改变免疫原性双链RNA的编辑水平来影响炎症性疾病的风险呢?Billy教授团队提出了如下假设:炎症性疾病的GWAS遗传变异对免疫原性双链RNA编辑的效应并不是随机的,而应具有明显的方向性。具体来说,遗传变异的两组等位基因中,保护等位基因(protective alleles)维持甚至升高目标免疫原性双链RNA的编辑水平,而风险等位基因(risk alleles)则相对的降低编辑水平。如此一来,富集了炎症性疾病GWAS遗传变异的个体体内将积累过多的、编辑不足的免疫原性双链RNA,进而激活MDA5并引发干扰素免疫应答,提高患病风险(图14)。
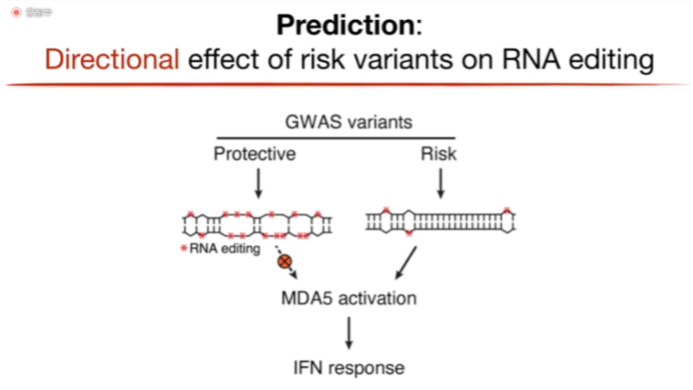
图14. 遗传变异通过改变免疫原性双链RNA编辑水平引发免疫反应的模式图
进一步分析发现dsRNA编辑水平的降低和干扰素反应水平呈正相关关系(图15)。Billy教授对这项工作进行的总结,由于遗传变异导致的dsRNA编辑水平的降低会通过激活MDA5来引发一些自身免疫病/炎症性疾病。
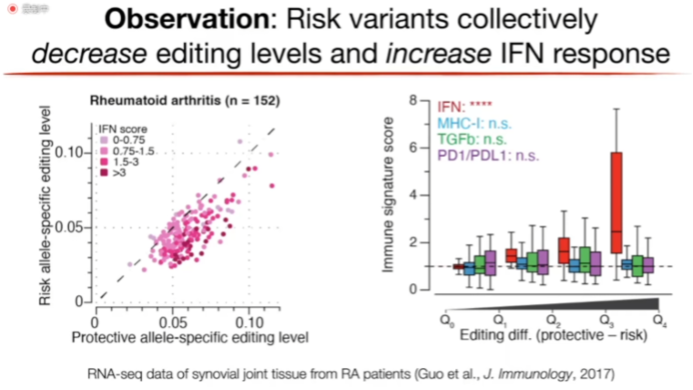
图15. dsRNA编辑水平的降低和干扰素反应水平的关系
最后,Billy教授总结了该领域这些年的一些发现,他认为genetics在整个领域的发展中是非常重要的,并希望在未来能够利用genetics来对病人进行分型,从而更好的进行治疗。从目前研究来看,可能可以通过上调dsRNA感受器的表达来治疗肿瘤或下调dsRNA感受器的表达来治疗炎症性疾病(图16)。
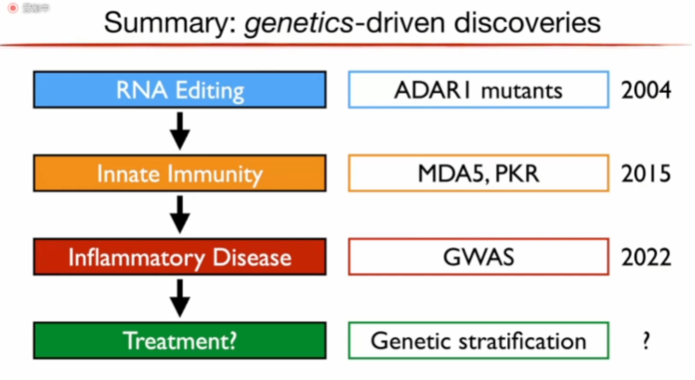
图16. 总结
此外,Billy教授还介绍了ADAR除了在疾病治疗中的应用以外还会在基因工程等领域中进行应用,例如可以利用ADAR进行突变的修复等(图17);同时与DNA编辑相比,RNA编辑会更安全等。
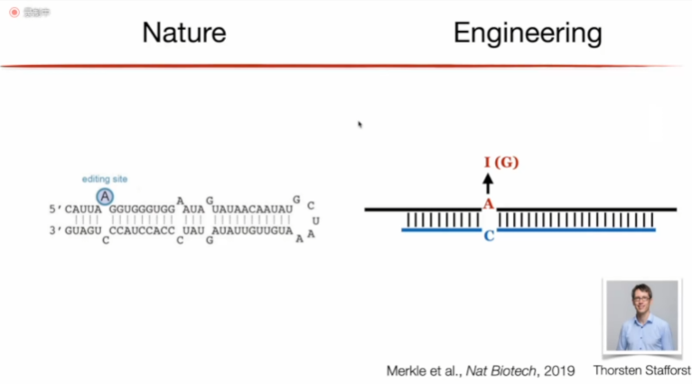
图17. 利用ADAR进行突变修复
精彩问答
首先陆剑老师提出了一个非常有意思的问题。他好奇当病毒感染以后,会不会竞争ADAR从而导致ADAR对自身dsRNA的编辑水平降低,从而加重自身免疫性疾病。对于该问题,Billy教授从两个角度进行回答,第一,当病毒进入细胞以后,ADAR会对病毒RNA进行编辑,从而导致自身dsRNA的编辑水平降低;第二,病毒被MDA5识别以后,产生的干扰素会激活ISG基因包括MDA5的表达,MDA5的表达水平会升高,因此自身dsRNA更容易被MDA5识别。但从进化角度来看,相对于自身免疫性疾病来说,对抗病毒往往是更加重要的,他相信这里面一定有一个很有趣的结合机制。
紧接着,陈炜老师提出了问题,他观察到在正常情况下ADAR1p110的表达量远高于p150,他很好奇p110的作用是不是主要是在核内binding的作用?针对该问题,Billy认为p110在核内的编辑功能不是最重要的;他认为有2个证据可以支撑这个结论,第1个证据是:在和Carl Walkley合作的研究中,将ADAR1的p150和p110都进行点突变使其丧失编辑功能并敲除MDA5后,小鼠就活正常的寿命,所以这样来看,p110的编辑功能没有那么重要;第2个证据是:日本一个团队发现只敲除ADAR1p110以后,有80%左右的老鼠在断奶前就死亡了,其它的都能活正常寿命;他们团队将ADAR1p110敲除的老鼠和 ADAR1p150和p110都进行E861A点突变的老鼠进行交配,出生的老鼠都能活正常的寿命,在这些老鼠中,p110都没有编辑功能,但小鼠仍然能活寿命,Billy教授认为ADAR1p110在核内的binding功能是非常重要的,但目前还没有弄清楚。
此外,还有很多老师和同学提出了精彩的问题。
李进(Jin Billy Li)教授此次会议报告已收录于Guangzhou RNA club bilibili视频网站(【李进 (Jin Billy Li)-RNA 编辑:先天性免疫和自身炎症性疾病】 https://www.bilibili.com/video/BV1LPHMefEp6/?share_source=copy_web)
欢迎关注Guangzhou RNA club公众号、网站(rnaclub.rnacentre.org)、twitter(@RNA_club)。
















